Mikrobiyoloji
AZİZ SANCAR FOTOLİYAZ ENZİMİ İLE DNA ONARIMI VE SİRKADİYEN RİTİM MEKANİZMASI
DNA molekülü üzerinde yapılan değişiklikler bilgilerin işlenme sürecinde kullanılan şifrenin değişikliğine yol açar ve protein üretimi gibi süreçler gerçekleşmez veya aksamaya uğrar. Fiziksel etkenler (UV ışınları gibi), DNA bozunmasına sebep olur. Eğer tamir edilmezse hücrede mutasyonlar birikir. Ayrıca replikasyon sırasında polimerazların hızlı bir şekilde bazları yerleştirmesi sonucu bazlar yanlış yerleştirilebilir ve bu sorunu DNA tamir mekanizması çözer. Bu şekilde genetik materyalin bütünlüğü bozulur. Bu bütünlüğün bozulmasına neden olan etmenlere endojen (spontan) ve eksojen (çevresel) faktörler denir. Bu faktörlerin etkisi ile meydana gelen ve onarılamayan tüm değişikliklere “DNA Hasarı” denir.1-2
Prof. Dr. Aziz SANCAR, Türk akademisyen, Biyokimyager, Moleküler Biyolog ve Bilim insanıdır. DNA onarım mekanizmasının birçok parçasının tanımlanmasında kullanılan biyokimyasal yaklaşımlara öncü olması ile tanınıyor. 2015 yılında hücrelerin hasar gören DNA’ları nasıl onardığını ve genetik bilgisinin nasıl korunduğunun haritalanması çalışmaları ile Nobel Kimya Ödülü’nü kazanmıştır. Prof. Dr. Aziz SANCAR, Fotoliyaz enzimi ile DNA’nın onarılma mekanizmalarını aydınlatmıştır.
DNA, fiziksel etkenler ile bozulmaya uğrayabilir. Bu fiziksel etken UV ışınları olabilir. UV ışınları, DNA’nın yapısında bulunan Timin bazları arasında kovalent bağlanma ile Timin dimerleri oluşur. Bu timin dimerlerini plasentalı memeliler hariç diğer organizmalarda DNA fotoliyazlar ile dimerler kesilir ve DNA üzerinde olan hasar onarılır. Normalde güneş ışığına maruz kalan derideki hücrelerde saniyede 50-100 timin dimeri oluşur. Fakat bu dimerler hemen kesilerek onarılır.DNA dimerleri eğer onarılmazsa, rekombinasyona etki ederek mutasyonların birikmesine ve kanserin ortaya çıkmasına neden olur. Deneyler sonucu bu meydana gelen timin dimerlerinin melanin sentezini 7 kat arttırdığı gözlemlenmiştir. Reaksiyonlarda her zaman denge önemlidir. Melanin sentezinin artışı bahsedildiği gibi olumsuz sonuçlara sebep olur.5-6
Fotoliyaz enzimi Claud S. Rupert tarafından keşfedilmiştir. Bu keşiften onlarca yıl önce UV ışınının bakterileri öldürdüğü bilinmektedir. Fotoliyaz, ışık enerjisini kullanır. UV ışınları tarafından DNA üzerinde timin dimerleri oluşur ve fotoliyaz oluşan dimerleri onarmak için mavi ışık fotonlarını kullanır. Cold Spring Harbor’dan Kelner, UV ışınları ile ölen bakteriler üzerinde görünür ışık uygulayarak tekrar yaşamaya başladıklarını gözlemlemiştir.5-6
Bu keşifler sonucunda, UV ışınlarının bakterilerin ölmesine neden olduğunu fakat bakteriler görünür ışıkta mavi ışık kullanan fotoliyaz enziminin aktivitesi sonucu ortaya çıkan DNA hasarının onarıldığını sonucuna varılmıştır. Mavi ışık ölü hücreler üzerinde canlandırıcı etkiye sahiptir.
UV ışını timin bazlarını ve iki tane yan yana bulunan pirimidini bir siklobütan pirimidin dimerine (CPD- Bundan sonra böyle bahsedilecektir.) dönüştürür. Mavi ışık enerjisi ile aktivite gösteren fotoliyaz enzimi, anormal bağlanma gösteren timin dimeri ve CPD’yi onararak normal hallerini geri kazandırır.
En büyük sorun E.coli hücrelerinden sadece 10-20 fotoliyaz molekülü elde ediliyor olduğundan hücreden fotoliyaz enzimi saflaştırılamıyor olmasıydı. Aziz Sancar’ın geliştirdiği Maxicell yöntemi klonlanan hücre kromozomu ile etkileşime giriyor, yalnızca istediğimiz ve klonladığımız protein ürününü elde etmemizi sağlıyor. Bu yöntem ile fotoliyaz enziminin çalışma mekanizmasının aydınlatılması daha da kolaylaşmıştır. Böylece fotoliyaz enzimi fazla sayıda üretilecek ve sonrasında saflaştırma işlemi daha kolay olacaktır.5-7
Fotoliyaz enzimi iki tane kofaktöre sahiptir. Fotoliyaz enziminin reaksiyon hızını arttırması için yardımcı molekül öncelikle FAD (Flavin adenin dinükleotid)dir diğeri ise metiltetrahidrofolat (MTHF) veya 8-hidroksi-7,8-dimetil-5-deaza-riboflavin (8-HDF)’dir.5
FAD, UV ışınlarından dolayı hasarlanmış olan DNA’ya spesifik olarak bağlanır ve kataliz için temel kofaktör görevine sahiptir. Enerji farkının görünür spektrumda olduğu bölgede sınırlayıcı ışık altında MTHF veya 8-HDF dalga boyu ile bağlı olarak onarımı 10-100 kat arttırır. MTHF ve 8-HDF’nin iki adet mavi ışık emici orbitali olduğu gösterilmiştir. MTHF güneş paneli gibi enzim üzerine oturur ve gelen ışığı emer. Emdiği ışık enerjisini FAD’a aktarır.5
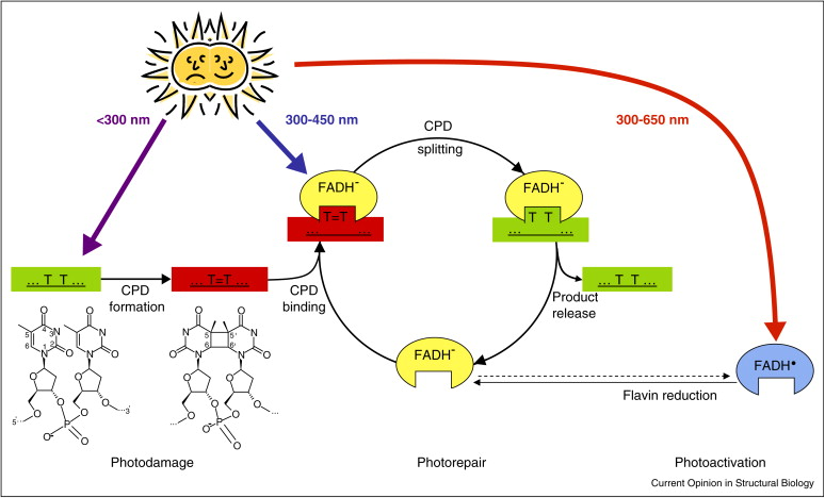
Şekil-1 (Fotoliyaz Enzim Mekanizması)
UV ışınları hücreye etki ettiğinde DNA üzerinde hasara neden olur. Işınlar, bitişik halde bulunan pirimidin bağları arasında siklobütan pirimidin dimerleri (CPD) oluşumunu indükler.8 CPD’ler DNA omurgasının bozunmasına neden olur. DNA negatif yüklü iskeleti ile fotoliyaz enziminin pozitif oluğu birleşir ve enzim DNA fosfodiester omurgasını kendi enzim çekirdeğine doğru çeker. Fotoliyaz enzimi, yapıya özgü DNA bağlayıcı bir proteindir. Enzim bu işlemi ışıktan bağımsız olarak gerçekleştirir. MTHF, enzimin üstüne çatı gibi oturur ve fotonları emerek katalitik reaksiyon başlatılır. Fotoliyaz enziminin kofaktörü olan FADH ile fotoliyaz enzimi Van der Walls kuvvetleri ile birbirine bağlıdır. Fotoliyaz ve FADH arasında temel bir kompleks oluşur. Folat (MTHF) bir foton emer ve bu ışık enerjisini Förster rezonans enerjisi (FRET) ile FADH’a aktarılır. 5
Uyarılmış durumda bulunan FADH, CPD’leri onarmak ve dimerleşmeyi ortadan kaldırmak için siklik redoks reaksiyonunu kullanarak dimerleri birbirinden ayırır. Onarılan pirimidin dimerlerinden enzim kompleksi ayrılır ve onarım reaksiyonuna devam etmek için diğer bölgelere göç eder. (Flavin indirgenmesi 300-650 nm dalga boylarında gerçekleşir.)5
G-C bakımından zengin bir sekansta dimerlerin iyileştirilmesi A-T bakımından zengin sekansa göre daha zordur. Bunun nedeni G ve C bazları arasında üçlü bağ olma durumundan dolayı olabilir.5
Kriptokom Nedir? Bu genin mutasyonu sonucu hangi hastalıklar meydana gelir?
Kriptokrom, bitkilerde mavi ışık tepkilerini düzenler. Büyüme ve gelişmede büyük role sahip önemli bir flavoprotein sınıfıdır. Hayvanlarda ise sirkadiyen ritim olarak adlandırılan 24 saatlik aydınlık-karanlık döngüsüne vücudumuzun biyokimyasal ve davranışsal olaylarını düzenlenmesini sağlar.9-10
Kriptokrom-1 (CRY-1) olarak adlandırılan gende mutasyonların gelişmesi sonucu gecikmiş uyku fazı veya DSPD (delayed sleep phase disorder) hastalığı gelişebilir. DSPD tanısı konulan bireyler geceleri uykuya dalmakta sıkıntı çekerler ve genelde uykuları şekerleme şeklinde aralıklı olarak gerçekleşir. CRY1 mutasyonu taşıyan kişilerde biyolojik saat düzeninin bozulduğu gözlemlenmiştir. 11
Biyolojik saat hücre içeriside “başlatıcı ve aktivatör” olarak yer alan proteinlerin birikmesi sonucu biyolojik saatimiz çalışmaya başlamaktadır. Başlatıcı proteinler de hücre içerisinde sentezlenir. CRY1 geni bu biyolojik döngüde durdurucu görev üstlenir. Fakat CRY1 geninde meydana gelen nokta mutasyonu ile bir bazın değişmesine yol açar ve CRY1’in görevini yapmasını engellemektedir. CRY1’in aktivitesi artar ve daha çok çalışmaya başlar bu durum uyku düzensizliğine yol açar. Ayrıca genetik açıdan bakıldığında CRY1 gen mutasyonu anne ve babadan dominant olarak kalıtıldığında uyku sorunları ortaya çıkar. 11
Biyolojik Saat Nedir ve Mekanizması?
Canlı organizmaların kendilerini düzenli bir ritime adapte etmek için yardımcı bir biyolojik saate ihtiyaç duyarlar. Günlük çevresel değişikliklere uyum sağlamamızı sağlayan iç saatimiz, hormon dengesinin düzenlenmesi, vücut ısısı ve metabolizma gibi kritik işlemleri bir düzen içerisinde yerine getirir. Bu 24 saatlik kontrol dört önemli protein tarafından kontrol edildiği deneyler ile gösterilmiştir. Bu proteinler Kriptokrom (CRY), Periyod (PRY), CLOCK ve BMAL1 proteinleridir. Biyolojik saatin negatif ve pozitif döngüler ile düzenlenmesi bu proteinlerin birbirleri arasında etkileşimleri sonucu ortaya çıkar.
CLOCK ve BMAL1 proteinleri, genin promotor bölgesine bağlanır ve pozitif bir döngü başlatır. Bu pozitif döngüyü kontrol eden ikili ise CRY-PRY’dir. Bu ikili gen ifadesini baskılar ve bu döngü 24 saat boyunca aynı şekilde devam eder.11-12
Sirkadiyen ritim çalışmaları ile 2017 yılında Nobel Tıp Ödülü’ne üç bilim insanı layık görülmüştür. Jeffrey C. Hall, Michael Rosbash, Michael W. Young.12
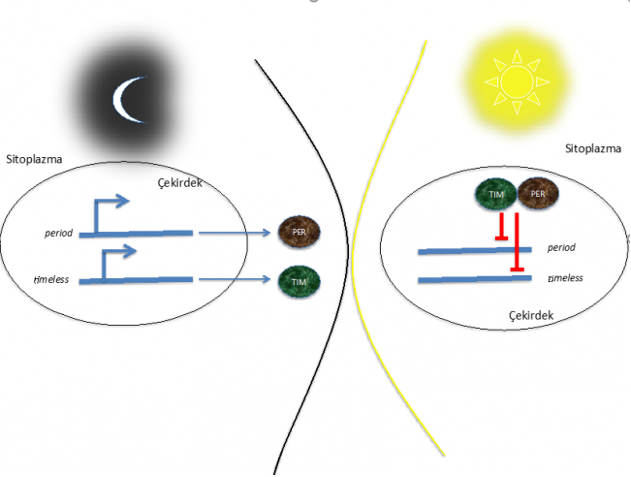
Şekil-2 (PER ve TIM proteinlerinin gece ve gündüz aktiviteleri gösterilmiştir.)
Nobel Ödülü alan çalışmada meyve sineği üzerinde çalışılmıştır. PRD geni üzerinde meydana gelen mutasyonların sirkadiyen ritmi bozduğu gösterilmiştir. Bu üç bilim insanı öncelikle meyve sineğinden PRD genini izole etmeyi başarmışlardır. PRD geni tarafından kodlanan PER proteinlerinin gece boyunca hücre çekirdeğinde biriktiği ve gündüz saatlerinde bozunduğu gösterilmiştir. PER proteinleri sirkadiyen ritim ile senkronize bir şekilde çalışır.12
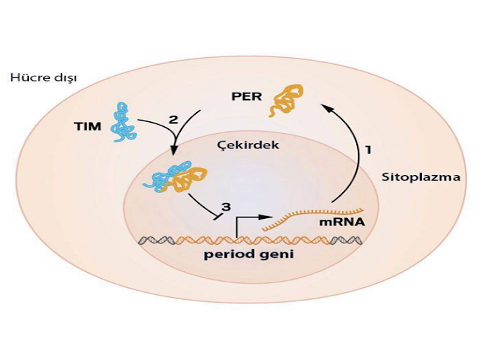
Şekil-3 (PER ve TIM proteinlerinin hücre içerisinde çalışma mekanizması gösterilmiştir.)
24 saatlik süre boyunca PRD proteini aktiftir ve sürekli mRNA yaparak mRNA’yı hücre sitoplazmasına gönderir. Protein hücre çekirdeğinde birikmeye başlandığında gen aktifliği engellenir. Bu negatif feedback mekanizmasıdır. Fakat bu negatif feedback’in gerçekleşmesi için PER proteinin genetik materyalini hücre çekirdeğine ulaştırması gerekir. Bunun için TIM proteinini kodlayan ikinci bir gen keşfedilmiştir. Timeless, TIM ve PER birbirlerine bağlandığında birlikte hücre çekirdeğine giriş yaptıklarını ve inhibitör olarak iş gören döngüyü kapatmak için PRD gen aktivitesini bloke ettikleri gösterilmiştir. Ayrıca salınımların sıklığını kontrol altında tutan bir PER proteini hücre çekirdeğinde birikimini geciktiren DBT protein kodlanmasını sağlayan doubletime geni tanımlanmıştır.12
REFERANS
- https://www.ncbi.nlm.nih.gov/books/NBK9900/
- Yılmaz Özden, T. DNA Hasarı ve Onarımı. İstanbul Üniversitesi
- https://tr.wikipedia.org/wiki/Aziz_Sancar
- https://services.tubitak.gov.tr/edergi/user/yaziForm1.pdf?cilt=49&sayi=897&sayfa=22&yaziid=38355
- Sancar, A. (2016). Mechanism of DNA Repair by Photolyase and Excision Nuclease (Nobel Lecture). DOI: 10.1002/anie.201601524
- Sancar, A. (2003). Structure and Function of DNA Photolyase and Cryptochrome Blue-Light Photoreceptors. Chemical Reviews. Vol.103 No.6.
- https://kurious.ku.edu.tr/aziz-sancar-turkiyeye-donerdim-ama/
- https://tr.wikipedia.org/wiki/Timin_ikilisi
- https://en.wikipedia.org/wiki/Cryptochrome
- https://genomebiology.biomedcentral.com/articles/10.1186/gb-2005-6-5-220
- https://w3.bilkent.edu.tr/www/gece-kusu-uyku-duzenine-neden-olan-genetik-mutasyon-bulundu/
- https://www.nobelprize.org/prizes/medicine/2017/press-release/




